Table des matières
Semaine du 30/05/22
1. Correction Activité p 60
2. Leçon
3. Transformation physique
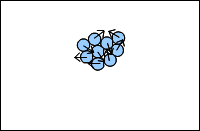
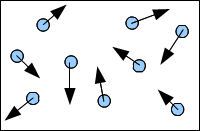
Lors d'une transformation physique, une substance change de forme ou d'aspect mais garde la même composition.
Les molécules restent identiques mais elles changent de disposition.
Ex : de l'eau liquide transformée en vapeur
II. La conservation de la masse
1. La conservation de la masse lors des mélanges en solutions aqueuses
La masse n'a pas varié.
Interprétation :
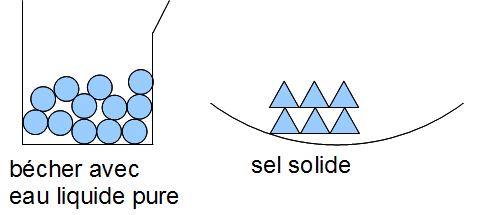
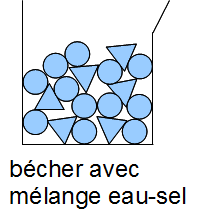
Le nombre de molécule ne change pas, donc la masse ne change pas non plus.
2. La conservation de la masse lors d'un changement d'état de l'eau (transformation physique)
La masse n'a pas varié.
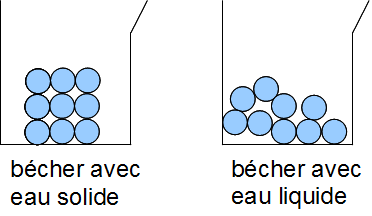
Le nombre de molécule ne change pas, donc la masse ne change pas non plus.
3. Conservation de la masse lors d'une transformation chimique
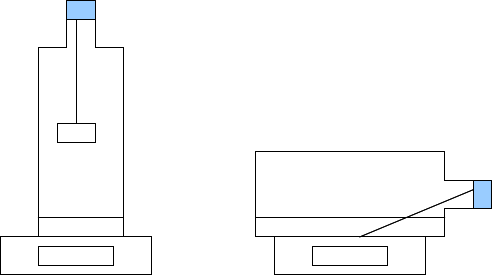
Lors d'une transformation chimique, la masse se conserve. Les molécules ont changé et on explique au chapitre suivant pourquoi cette masse ne varie pas.
3. Activité à faire en classe
Activité p 74
Activité p 74
1. 1 atome d'oxygène et 2 atome d'hydrogène
2. Atome d'oxygène : O (boule rouge)
Atome d'azote : N (boule bleue)
Atome de carbone : C (boule noire)
3.
| Nom | représentation | formule | composition atomique |
|---|---|---|---|
| dioxygène | 2 boules rouges | 02 | 2 atomes d'oxygène |
| diazote | 2 boules bleues | N2 | 2 atomes d'azote |
| dihydrogène | 2 boules blanches | H2 | 2 atomes d'hydrogène |
| dioxyde de carbone | 1 boule noire 2 boules rouges | CO2 | 1 atome de carbone 2 atomes d'oxygène |
4. Une molécule est composée d'atomes
On la représente par des boules de couleurs (modèle moléculaire) et une formule chimique.
4. A faire pour la prochaine fois
Activité p 75